近日,在國家自然科學基金、福建省自然科學基金重點項目以及中國科學院福建物質結構研究所(以下簡稱:福建物構所)“前瞻跨越”計劃揭榜掛帥項目等多項科研項目支持下,福建物構所陳卓課題組在雙特異性納米抗體研發中取得重要突破,為攻克腫瘤耐藥性和轉移難題提供了創新解決方案。相關研究成果以“Transient intracellular expression of PD-L1 and VEGFR2 bispecific nanobody in cancer cells inspires long-term T cell activation and infiltration to combat tumor and inhibit cancer metastasis”為題,發表于Molecular Cancer(DOI: 10.1186/s12943-025-02253-6)。福建物構所陳卓研究員、張蕾研究員及中山大學附屬第一醫院柯尊富教授為共同通訊作者。張蕾研究員與福建農林大學-中國科學院福建物質結構研究所聯合培養碩士生林云鳳為共同第一作者。
研究團隊創新性設計出可同時靶向PD-L1和VEGFR2的雙特異性納米抗體FAP1V2。該抗體通過基因工程改造,僅保留抗體重鏈可變區(VH),形成僅約15kDa的納米級結構,較傳統單抗(150kDa)體積縮小10倍,展現出三大顯著優勢:1)深度滲透:納米尺寸使其更易穿透腫瘤致密間質,直達病灶核心;2)雙重阻斷:同步抑制PD-L1/PD-1免疫檢查點信號和VEGFR2介導的腫瘤血管生成及轉移通路;3)低免疫原性:經優化的蛋白結構顯著減少人體免疫系統識別風險。在小鼠乳腺癌模型中,FAP1V2展現出顯著的協同干預效能。實驗數據顯示,經FAP1V2處理的小鼠原發腫瘤體積較對照組縮小68%,肺、肝轉移灶數量銳減82%,腫瘤微環境中效應T細胞(TCR βhi/CD25hi亞群)浸潤密度提升4.3倍。值得注意的是,部分實驗小鼠在二次接種同種腫瘤細胞后,免疫系統展現出強大的記憶效應,成功實現腫瘤完全排斥。
分子機制研究揭示,FAP1V2通過精準調控腫瘤信號網絡發揮治療作用。轉錄組分析表明,該抗體顯著抑制Wnt/β-catenin經典通路,阻斷腫瘤干細胞自我更新能力;同時靶向MET-PI3K信號軸,削弱腫瘤細胞的侵襲遷移潛能。雙重通路抑制協同下調腫瘤干細胞標志物CD44表達,顯著削弱腫瘤轉移的種子細胞庫。這項研究不僅驗證了雙靶點納米抗體的技術可行性,更揭示了其重塑腫瘤微環境的獨特優勢。FAP1V2如同“分子剪刀”,精準剪斷腫瘤逃逸的雙重保險——免疫抑制和轉移信號,為開發新一代免疫聯合療法提供了核心元件。目前,團隊正基于FAP1V2開發靶向遞送系統,探索其與CAR-T細胞療法、溶瘤病毒等技術的聯用潛力。未來將聯合多種前沿腫瘤治療手段,推動個性化癌癥治療方案的優化。
該研究團隊長期專注于癌癥發生機制及免疫治療領域的研究探索,近年來在相關學術領域取得了豐碩成果,其研究成果相繼發表于國際知名學術期刊,包括Molecular Cancer (2020,19:10;2022,21: 103)、Acta Pharmaceutica Sinica B (2023,13: 982) 以及Cancer Letters (2023,563: 216181)等刊物上發表了一系列具有重要影響力的研究論文。
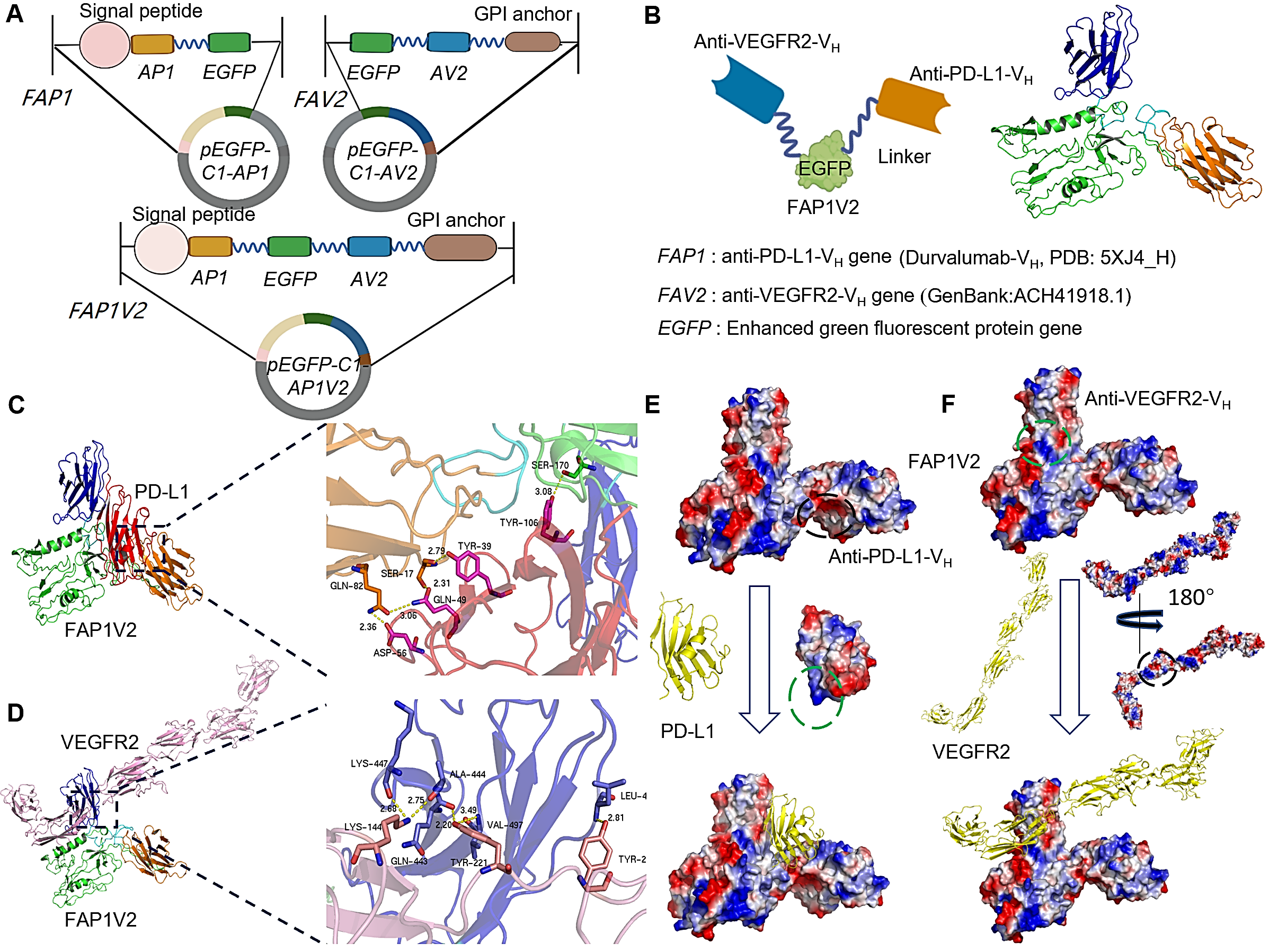
圖1.復合物FAP1V2/PD-L1及FAP1V2/VEGFR2的胞內抗體設計及分子對接。(A)重組雙特異性胞內抗體基因(FAP1V2)序列包含IL-2信號肽、抗PD-L1 VH基因(AP1)和抗VEGFR2 VH基因(AV2)、EGFP報告基因以及GPI錨定序列。pEGFP-C1-AP1攜帶FAP1,pEGFP-C1-AV2攜帶FAV2。(B)FAP1V2的三維模型。橙色區域表示抗PD-L1 VH(AP1);深藍色區域表示抗VEGFR2 VH(AV2);綠色區域表示EGFP,其通過(GGGGS)?連接子(以淺藍色顯示)分別與抗PD-L1 VH和抗VEGFR2 VH融合。(C)和(D)分別為FAP1V2與PD-L1(紅色)和VEGFR2-ECD(粉色)的分子對接及結合位點預測。(E)FAP1V2與PD-L1間接觸電位。(F)FAP1V2與VEGFR2間接觸電位。正電荷區域用黑色圓圈標出,負電荷區域用綠色圓圈標出。靜電表面圖中,藍色和紅色分別代表中性pH條件下所呈現的正靜電電位和負靜電電位。

 主站蜘蛛池模板:
迭部县|
泗阳县|
海原县|
抚顺县|
原平市|
昭苏县|
龙江县|
万宁市|
峡江县|
常德市|
武宣县|
怀来县|
怀化市|
梁平县|
河曲县|
永善县|
安吉县|
德钦县|
塔河县|
长宁区|
塔城市|
普宁市|
呼玛县|
陆良县|
磐石市|
科技|
桓仁|
织金县|
咸阳市|
十堰市|
张家港市|
喜德县|
郑州市|
贺兰县|
旌德县|
德昌县|
罗江县|
郯城县|
富阳市|
永胜县|
永安市|
主站蜘蛛池模板:
迭部县|
泗阳县|
海原县|
抚顺县|
原平市|
昭苏县|
龙江县|
万宁市|
峡江县|
常德市|
武宣县|
怀来县|
怀化市|
梁平县|
河曲县|
永善县|
安吉县|
德钦县|
塔河县|
长宁区|
塔城市|
普宁市|
呼玛县|
陆良县|
磐石市|
科技|
桓仁|
织金县|
咸阳市|
十堰市|
张家港市|
喜德县|
郑州市|
贺兰县|
旌德县|
德昌县|
罗江县|
郯城县|
富阳市|
永胜县|
永安市|